Noticias
Anvisa aprova produto de terapia avançada para tratamento de câncer
Agência Nacional de Vigilância Sanitária (Anvisa) aprovou, nesta quarta-feira (23), o primeiro registro sanitário no país de tratamento avançado para câncer hematológico. O produto da empresa Novartis é uma terapia gênica baseada em células T de receptores de antígenos quiméricos (CAR), as chamadas “células CAR-T”.
O Kymriah (tisagenlecleucel) faz parte de uma nova geração de imunoterapias personalizadas contra o câncer, que se baseiam na coleta e na modificação genética de células imunes dos próprios pacientes.
As células T do paciente são coletadas no serviço de saúde e enviadas para um centro de fabricação, onde são geneticamente modificadas, incluindo-se um novo gene que contém uma proteína específica (um receptor de antígeno quimérico ou CAR).
É justamente essa proteína que direciona as células T para matar células do câncer que apresentem um antígeno específico (CD19) em sua superfície. Depois de modificadas no laboratório, as células são cultivadas e formuladas em suspensão farmacêutica para compor o produto que será aplicado no paciente.
O produto aprovado pela Anvisa é indicado para o tratamento de pacientes pediátricos e adultos jovens (até 25 anos de idade) com Leucemia Linfoblástica Aguda (LLA) de células B, refratária ou a partir da segunda recidiva. O tratamento está igualmente indicado para pacientes adultos com Linfoma Difuso de Grandes Células B (LDGCB) recidivado ou refratário, após duas ou mais linhas de terapia sistêmica.
O produto foi também aprovado por outras autoridades regulatórias, como a Food and Drug Administration (FDA), nos Estados Unidos; a European Medicines Agency (EMA), na Europa; e a Pharmaceuticals and Medical Devices Agency (PMDA), no Japão.
Processo de avaliação
De acordo com a Anvisa, as análises feitas apontaram que o complexo processo de produção, transporte, administração e monitoramento pós-uso do produto é seguro e promove a eficácia pretendida. Os benefícios do tisagenlecleucel foram considerados superiores aos seus riscos.
Foram 268 dias corridos de avaliação, desde a submissão dos documentos pela Novartis à Anvisa até a publicação do registro, considerando os prazos de análise dos profissionais da agência e das respostas ao cumprimento das exigências por parte da empresa.
Fonte: CNN Brasil
-

 Iguatu1 semana atrás
Iguatu1 semana atrásDeputado Marcos Sobreira vota contra emenda para tratamento oncológico em Iguatu e decisão gera forte reação
-

 Brasil1 semana atrás
Brasil1 semana atrásTrabalhadores processam Volkswagen por regime análogo à escravidão; Ministério aponta incentivos da ditadura
-

 Iguatu2 semanas atrás
Iguatu2 semanas atrásIGUATU – PRESIDENTE DO CONSELHO MUNICIPAL DE EDUCAÇÃO É DEMITIDO APÓS CONDENAÇÃO POR FALSIFICAÇÃO DE DOCUMENTOS
-

 Iguatu1 semana atrás
Iguatu1 semana atrásEnquanto o Governo do Ceará amplia o Sinalize, Iguatu arrecada milhões em IPVA e mantém ruas esburacadas
-

 Ceará1 semana atrás
Ceará1 semana atrás‘Até que a morte os separe’: em 80% dos feminicídios o autor é o companheiro ou ex da vítima
-
 Ceará1 semana atrás
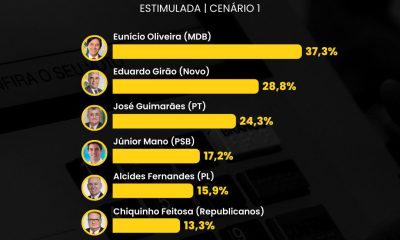
Ceará1 semana atrásPesquisa do Instituto Paraná Pesquisas aponta Eunício Oliveira na liderança para o Senado no Ceará
-

 Iguatu2 semanas atrás
Iguatu2 semanas atrásJustiça proíbe rádio de Iguatu (CE) de tocar músicas e cobra R$ 971 mil em ação por não pagamento de direitos autorais
-

 Brasil1 semana atrás
Brasil1 semana atrásVITÓRIA CONTRA O MARCO TEMPORAL: STF forma maioria e derruba tese que restringe direitos indígenas